Los pacientes de trasplantes suelen quedarse en el hospital entre 4 y 6 semanas o más. Su hijo(a) se quedará en una parte especial del hospital para pacientes de trasplantes y otros pacientes con sistemas inmunitarios total o casi totalmente suprimidos. Las pautas de control de infecciones en la unidad de trasplante son diferentes de las de otras áreas del hospital.
Infusión de células madre
El proceso de trasplante es desafiante. Pero recibir células madre es relativamente simple. Es muy parecido a una transfusión de sangre. Las células madre están en una bolsa o jeringa conectada por una sonda a la vía central de su hijo(a). Tarda entre unos minutos y unas horas. No duele.
Incorporación del injerto
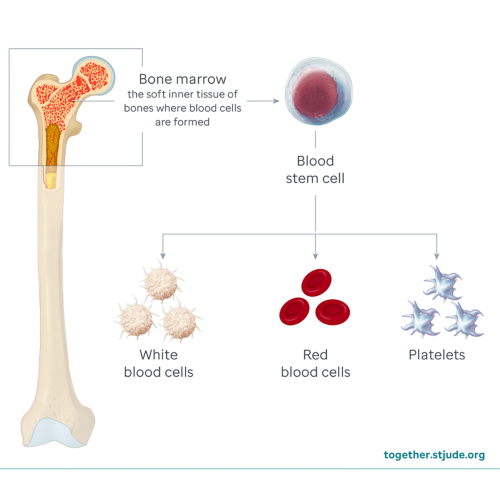
Luego de entrar en el torrente sanguíneo, las células madre viajan a la médula ósea. Aquí comienzan a dividirse. Las células madre se convierten en glóbulos rojos, glóbulos rojos y plaquetas. El proceso se llama incorporación del injerto. La incorporación del injerto suele comenzar después de entre 2 y 4 semanas de haber recibido las células. Los glóbulos blancos son los primeros en incorporarse, seguidos de los glóbulos rojos y luego las plaquetas. Es posible que su hijo(a) necesite trasfusiones de glóbulos rojos y plaquetas para mantener el recuento dentro de valores seguros mientras espera la incorporación del injerto.
Los médicos utilizan análisis de sangre para confirmar que se están generando células sanguíneas nuevas. Después del trasplante, su hijo(a) tendrá extracciones de sangre diarias para realizar pruebas. Su equipo de atención médica monitoreará los glóbulos rojos, glóbulos blancos y plaquetas de su hijo(a) para hacer seguimiento del progreso.
El aspirado de médula ósea también puede ayudar a los médicos a ver cuán bien están creciendo las células madre. Este procedimiento involucra la extracción de una muestra pequeña de médula ósea mediante una aguja para examinarla con el microscopio.
El cuidado de su hijo(a)
Un padre/madre u otro adulto de la familia deberá quedarse con su hijo(a) en el hospital. El proceso de trasplante es desgastante física y emocionalmente para los cuidadores. Es mejor tener más de un familiar cuidador que pueda cuidar de su hijo(a). Cada cuidador debe recibir capacitación, de modo que es importante planificar con antelación.
Prevención de infecciones
Durante la primera parte de la hospitalización, su hijo(a) recibirá quimioterapia de dosis alta con o sin radiación. El tratamiento deja espacio para las células madre sanas y ayuda a prevenir el rechazo de las células del donador. También debilita el sistema inmunitario, de modo que su hijo(a) estará en alto riesgo de tener una infección.
Los pacientes y los familiares cuidadores tienen que tomar muchas precauciones para prevenir infecciones, tales como usar una máscara y [g3]lavarse las manos[/g3] regularmente.
Se deben realizar exámenes a todos los visitantes para detectar posibles infecciones y enfermedades contagiosas. Todo centro de trasplantes es diferente. Sea consciente de las reglas del hospital para los visitantes.
Las pautas generales de la unidad de trasplante incluyen las siguientes:
- Los cuidadores y los visitantes deben cumplir ciertas pruebas de detección antes de ingresar a la unidad de trasplante y deben seguir las pautas de control de infecciones.
- Solo el paciente y un familiar cuidador pueden quedarse durante la noche.
- Las horas de visitas son limitadas. El cuidador principal no se considera una visita.
- En la mayoría de los casos, la cantidad de cuidadores y visitantes que se permite en la habitación es limitada.
- Es posible que haya requisitos de edad para los hermanos y visitantes.
- Todos los cuidadores y las visitas deben lavarse las manos al entrar y al salir de la habitación del paciente.
Apoyar a su hijo(a) durante el trasplante
Estar lejos de la familia, los amigos y las actividades normales puede ser difícil. El equipo de atención médica de su hijo(a) lo ayudará a estar tan cómodo(a) como sea posible. Los especialistas en vida infantil pueden proporcionar actividades divertidas tales como juegos y manualidades. Los terapeutas de rehabilitación crearán un plan de ejercicios para su hijo(a) y le dará ideas sobre cómo permanecer activo(a).
Puede traer juguetes y otros artículos para ayudar a su hijo(a) a sentirse más en casa. Anime a su hijo(a) a conectar con otras personas mediante mensajes de texto, redes sociales, videollamadas, llamadas telefónicas y cartas.
Mantenerse al día con la escuela
Su hijo(a) no podrá asistir a la escuela durante el trasplante y hasta que su sistema inmunitario se haya recuperado. Su hijo(a) se mantendrá al día con algunos deberes de la escuela. Converse con la escuela de su hijo(a) y conecte con los servicios escolares del hospital.