Пациенты, перенесшие трансплантацию, обычно находятся в больнице 4-6 недель или дольше. Ваш ребенок будет находиться в специальном отделении больницы для пациентов, перенесших трансплантацию, и других пациентов, у которых иммунная система работает слабо или вообще не работает. В отделении трансплантологии правила инфекционного контроля отличаются от правил, действующих в других отделениях больницы.
Инфузия стволовых клеток
Процесс трансплантации очень сложный. Но получить стволовые клетки довольно просто. Он очень похож на переливание крови. Стволовые клетки находятся в пакете или шприце, подключенном через трубку к центральному катетеру вашего ребенка. Это занимает от нескольких минут до нескольких часов. Это не больно.
Приживление
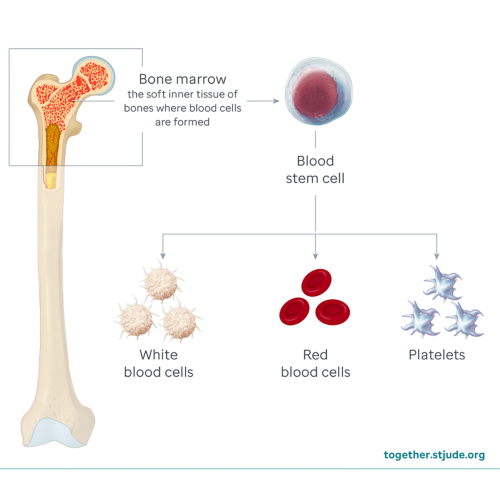
Попадая в кровь, стволовые клетки перемещаются в костный мозг. Здесь они начинают разделяться. Стволовые клетки превращаются в лейкоциты, эритроциты и тромбоциты. Этот процесс называется приживлением.
Приживление обычно начинается через 2-4 недели после получения клеток. Первыми приживляются лейкоциты, затем — эритроциты, а после — тромбоциты. Вашему ребенку могут потребоваться переливания эритроцитов и тромбоцитов, чтобы поддерживать их количество в безопасном диапазоне в ожидании приживления.
Врачи используют анализы крови, чтобы подтвердить, что образуются новые кровяные клетки. После трансплантации у вашего ребенка будут ежедневно брать кровь на анализ. Ваша команда врачей будет следить за уровнем эритроцитов, лейкоцитов и тромбоцитов в крови вашего ребенка, чтобы отслеживать прогресс.
Аспирация костного мозга также может помочь врачам увидеть, насколько хорошо растут новые стволовые клетки. В ходе этой процедуры через иглу удаляется небольшой образец костного мозга для исследования под микроскопом.
Забота о вашем ребенке
Один из родителей или другой взрослый член семьи должен будет находиться с вашим ребенком в больнице. Процесс трансплантации физически и эмоционально истощает тех, кто ухаживает за больным. Лучше всего, если за вашим ребенком будет ухаживать несколько родственников. Каждый ухаживающий за больным должен пройти обучение, поэтому важно планировать все заранее.
Профилактика инфекций
На начальном этапе госпитализации вашему ребенку будет проводиться высокодозная химиотерапия с лучевой терапией или без нее. Лечение создает пространство для здоровых стволовых клеток и помогает предотвратить отторжение донорских клеток. Это также ослабляет иммунную систему, поэтому ваш ребенок будет подвержен риску заразиться инфекцией.
Пациенты и те, кто ухаживает за ними, должны соблюдать множество мер предосторожности, чтобы предотвратить заражение, например, носить маску и часто мыть руки .
Все посетители должны проходить скрининг на возможные инфекции и инфекционные заболевания. Каждый центр трансплантации индивидуален. Ознакомьтесь с правилами посещения больницы.
Общие рекомендации для отделения трансплантологии включают следующее:
- Все лица, осуществляющие уход, и посетители должны соответствовать определенным критериям проверки, прежде чем попасть в отделение трансплантологии, и соблюдать правила инфекционного контроля.
- Только пациент и член семьи, осуществляющий уход, могут остаться на ночь.
- Часы посещения ограничены. Лицо, осуществляющее основной уход, не считается посетителем.
- Число ухаживающих лиц и посетителей, которым разрешено заходить в палату, ограничено.
- В отношении братьев и сестер, а также посетителей могут быть установлены возрастные ограничения.
- Все лица, ухаживающие за пациентом, и посетители должны мыть руки, когда входят и выходят из палаты пациента.
Поддержка вашего ребенка во время трансплантации
Расставание с семьей, друзьями и привычным образом жизни может быть тяжелым. Команда врачей поможет вашему ребенку чувствовать себя максимально комфортно. Специалисты по адаптации ребенка могут проводить развлекательные мероприятия, например игры или занятия творчеством. Реабилитационные терапевты составят план упражнений для вашего ребенка и дадут идеи о том, как оставаться активным.
Вы можете принести игрушки и другие предметы, чтобы ваш ребенок чувствовал себя как дома. Поощряйте ребенка общаться с другими людьми с помощью текстовых сообщений, социальных сетей, видеочатов, электронной почты, телефонных звонков и писем.
Сохранение успеваемости в школе
Ваш ребенок не сможет посещать школу во время трансплантации и до тех пор, пока его иммунная система не восстановится. Ваш ребенок может успевать выполнять некоторые школьные задания. Поговорите с руководством школы вашего ребенка и свяжитесь со школьной службой вашей больницы.