Les patients ayant subi une greffe restent généralement à l'hôpital pendant 4 à 6 semaines ou plus. Votre enfant restera dans une partie spéciale de l'hôpital pour les patients greffés et d'autres patients dont la fonction du système immunitaire est faible ou nulle. Les directives de contrôle des infections de l’unité de greffe sont différentes des autres zones de l'hôpital.
Perfusion de cellules souches
Le processus de greffe est difficile. Mais recevoir les cellules souches est relativement simple. C'est similaire à une transfusion sanguine. Les cellules souches se trouvent dans un sac ou une seringue reliée par un tube à la ligne centralede votre enfant. Cela prend quelques minutes à quelques heures. Ce n’est pas douloureux.
Prise de greffe
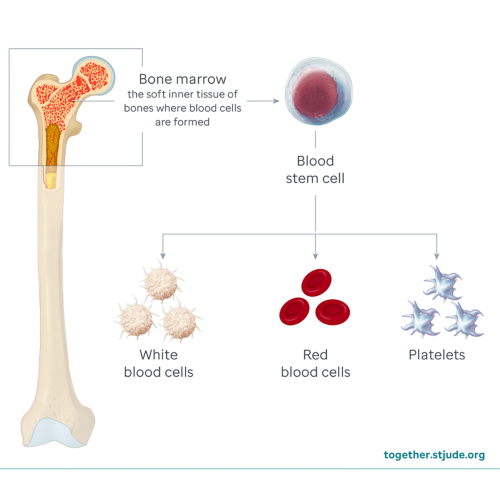
Après être entrées dans la circulation sanguine, les cellules souches se déplacent vers la moelle osseuse. Ici, elles commencent à se diviser. Les cellules souches deviennent des globules blancs, des globules rouges et des plaquettes. Ce processus s'appelle la prise de greffe. La prise de greffe commence généralement 2 à 4 semaines après que vous avez reçu les cellules. Les globules blancs sont les premiers à se greffer, suivis des globules rouges, puis des plaquettes. Votre enfant peut avoir besoin de transfusions de globules rouges et de plaquettes pour maintenir la numération dans une plage normale en attendant la prise de la greffe.
Les médecins utilisent des tests sanguins pour confirmer que de nouvelles cellules sanguines sont produites. Après la greffe, votre enfant aura des prélèvements sanguins quotidiens pour des tests. Votre équipe de soins surveillera les globules rouges, les globules blancs et les plaquettes de votre enfant afin de suivre les progrès.
La ponction de moelle osseuse peut également aider les médecins à voir comment les nouvelles cellules souches se développent. Cette procédure implique l'élimination d'un petit échantillon de moelle osseuse à l'aide d'une aiguille pour un examen au microscope.
Prendre soin de votre enfant
Un parent ou un autre membre adulte de la famille devra rester avec votre enfant à l'hôpital. Le processus de greffe est épuisant physiquement et émotionnellement pour les aidants. Il est préférable d'avoir plus d'un aidant familial qui peut s'occuper de votre enfant. Chaque auxiliaire de vie doit être formé, il est donc important de planifier à l'avance.
Prévention des infections
Au cours de la première partie du séjour à l'hôpital, votre enfant recevra une chimiothérapie intensive avec ou sans radiothérapie. Le traitement fait de la place pour les cellules souches saines et aide à prévenir le rejet des cellules du donneur. Cela affaiblit également le système immunitaire, donc votre enfant sera à haut risque de contracter une infection.
Les patients et les aidants familiaux doivent prendre de nombreuses précautions pour prévenir les infections, comme porter un masque et se laver souvent les mains.
Tous les visiteurs doivent être dépistés pour des infections possibles et des maladies contagieuses. Chaque centre de greffe est différent. Soyez conscient des règles de l'hôpital pour les visiteurs.
Les lignes directrices générales de l'unité de greffe incluent :
- Tous les aidants et les visiteurs doivent remplir certains critères de sélection avant d'être admis dans l'unité de greffe et doivent suivre les directives de contrôle des infections.
- Seuls le patient et l'aidant familial peuvent rester pendant la nuit.
- Les heures de visite sont limitées. L'aidant principal n'est pas considéré comme un visiteur.
- Le nombre d'aidants et de visiteurs autorisés dans la chambre est généralement limité.
- Il peut y avoir des exigences d'âge pour les frères et sœurs et les visiteurs.
- Tous les aidants et les visiteurs doivent se laver les mains lorsqu'ils entrent et sortent de la chambre du patient.
Soutenir votre enfant pendant la greffe
Être éloigné de sa famille, de ses amis et de ses activités normales peut être difficile. L'équipe de soins de votre enfant aidera votre enfant à être aussi confortable que possible. Les spécialistes de l'enfance peuvent proposer des activités amusantes telles que des jeux et des activités manuelles. Les thérapeutes en réhabilitation créeront un plan d'exercices pour votre enfant et donneront des idées sur la manière de rester actif.
Vous pouvez apporter des jouets et d'autres objets pour aider votre enfant à se sentir plus chez lui. Encouragez votre enfant à se connecter avec les autres par le biais de messages, de réseaux sociaux, de discussions vidéo, d'e-mails, d'appels téléphoniques et de lettres.
Poursuivre sa scolarité
Votre enfant ne pourra pas aller à l'école pendant la greffe et jusqu'à ce que son système immunitaire se soit rétabli. Votre enfant peut suivre certains travaux scolaires. Parlez à l'école de votre enfant et contactez les services scolaires de votre hôpital.