मेन्यू
बंद करना
एक्यूट लिम्फोब्लास्टिक ल्यूकेमिया (एएलएल) खून और बोन मैरो में होने वाला एक कैंसर है। यह बचपन में होने वाला सबसे सामान्य प्रकार का कैंसर है।
अमेरिका में हर साल 20 वर्ष से कम उम्र के लगभग 3,000 बच्चों और किशोरों में एएलएल रोग की पहचान की जाती है।
एएलएल अक्सर 2 से 5 वर्ष की आयु के बच्चों में होता है। यह बड़े बच्चों और किशोरों में भी हो सकता है। यह लड़कियों की बजाय लड़कों को थोड़ा ज्यादा प्रभावित करता है।
शिशुओं में एएलएल दुर्लभ है। अमेरिका में हर साल 1 वर्ष से कम उम्र के बच्चों में एएलएल के लगभग 90 मामलों की पहचान की जाती है।
एएलएल के लिए सबसे सामान्य इलाज कीमोथेरेपी है। एएलएल के इलाज में बहुत प्रगति हुई है। बच्चों में एएलएल के लिए समग्र इलाज दर लगभग 90% है।
खून के कैंसर (ल्यूकेमिया) में, कैंसर की कोशिकाएँ बोन मैरो में तेजी से बढ़ती हैं। ये कैंसर कोशिकाएँ अपरिपक्व सफेद रक्त कोशिकाएँ होती हैं जिन्हें ब्लास्ट कहा जाता है। जब ऐसा होता है, तो स्वस्थ रक्त कोशिकाएँ — सफेद रक्त कोशिकाएँ, लाल रक्त कोशिकाएँ और प्लेटलेट्स — अपना काम ठीक से नहीं कर पाती हैं।
एएलएल, सफेद रक्त कोशिकाओं को प्रभावित करता है, जिन्हें लिंफोसाइट कहा जाता है। ये कोशिकाएँ संक्रमण से लड़ती हैं और शरीर को बीमारी से बचाने में मदद करती हैं।
लिंफोसाइट दो प्रकार के होते हैं: बी-लिंफोसाइट और टी-लिंफोसाइट। एएलएल दोनों में से किसी भी लिंफोसाइट से उत्पन्न हो सकता है, इसलिए एएलएल के मामले या तो बी-सेल या फिर टी सेल एएलएल के रूप में जाने जाते हैं। बी-सेल एएलएल सबसे आम कैंसर है।
एएलएल के अधिकांश मामलों का कोई ज्ञात कारण नहीं होता है।
कुछ वंशानुगत सिंड्रोम एएलएल के बढ़े हुए जोखिम से जुड़े होते हैं।
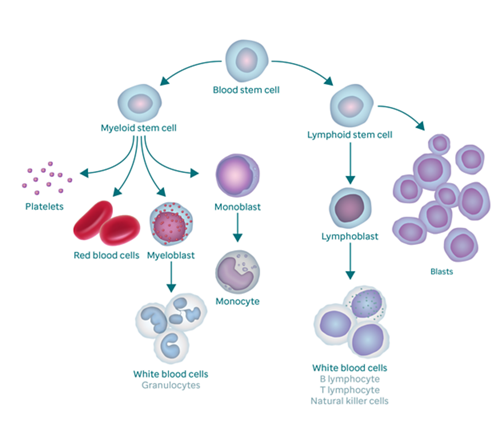
एएलएल, सफेद रक्त कोशिकाओं को प्रभावित करता है, जिन्हें लिंफोसाइट कहा जाता है। एएलएल से पीड़ित रोगियों के बोन मैरो में अत्यधिक मात्रा में अपरिपक्व सफेद रक्त कोशिकाएँ (ब्लास्ट) होती हैं। ये कोशिकाएँ सामान्य रूप से काम नहीं करती हैं। ये सामान्य सफेद रक्त कोशिकाओं, लाल रक्त कोशिकाओं और प्लेटलेट्स को हटा कर उनका स्थान लेती हैं।
एक्यूट ल्यूकेमिया (खून का कैंसर) से तात्पर्य है कि लक्षण तेजी से बिगड़ते हैं।
इससे बच्चे बहुत बीमार पड़ सकते हैं और उन्हें तुरंत चिकित्सा देखभाल की आवश्यकता पड़ सकती है।
एएलएल के निम्नलिखित संकेत और लक्षण हो सकते हैं:
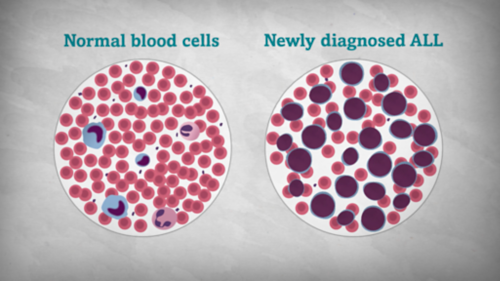
खून का कैंसर (ल्यूकेमिया) से पीड़ित बच्चों के खून में आमतौर पर सफेद रक्त कोशिकाओं की संख्या बहुत अधिक होती है।
कई बार शारीरिक जांच करके, चिकित्सकीय इतिहास जान कर और खून की जाँच के परिणामों को देखने के बाद चिकित्सकों को ल्यूकेमिया (खून का कैंसर) का संदेह हो सकता है।
ल्यूकेमिया (खून का कैंसर) रोग की पहचान की पुष्टि करने के लिए बोन मैरो जाँच की आवश्यकता होती है।
यदि ल्यूकेमिया (खून का कैंसर) पाया जाता है, तो यह पता लगाने के लिए कि क्या एएलएल शरीर के अन्य भागों में है और एएलएल के उपप्रकार के बारे में जानकारी एकत्र करने के लिए अतिरिक्त जाँचें की जाएंगी।
कैंसर रोग की पहचान होने पर, कैंसर के सही उपप्रकार का पता लगाने के लिए बोन मैरो पर और अधिक जाँचें की जाएंगी।
देखभाल टीम यह पता लगाने के लिए जाँच करेगी कि यह शरीर के अन्य भागों में है या नहीं।
एक लंबर पंक्चर दिखाएगा कि क्या खून का कैंसर केंद्रीय तंत्रिका तंत्र में फैला है या नहीं। इस जाँच को LP या स्पाइनल टैप (रीढ़ की हड्डी के अंदर से पानी निकालना) भी कहा जाता है।
रोगियों को उसी समय कीमोथेरेपी दी जा सकती है जब यह प्रक्रिया की जाती है। इसे रोग निरोधक इंट्राथेकल कीमोथेरेपी कहा जाता है। यह एएलएल को रीढ़ की हड्डी में पानी में फ़ैलने से रोकने के लिए दिया जाता है।
छाती का एक्स-रे यह देखने के लिए किया जाएगा कि क्या खून के कैंसर (ल्यूकेमिया) वाली कोशिकाओं से छाती के बीच में कोई पिंड बना है।
यदि रोगियों में कुछ संकेत और लक्षण हों तो अन्य इमेजिंग अध्ययन और लेबोरेट्री जाँच की जा सकती हैं।
प्रसव आयु वाली महिला रोगियों की गर्भावस्था जाँच हो सकती है।
चिकित्सक को वीर्यकोष की भागीदारी का संदेह होने पर पुरुष रोगियों की अल्ट्रासाउंड द्वारा जाँच की जा सकती है। एएलएल में यह दुर्लभ है। यह 1-2% पुरुषों में होता है।
विशेष रूप से किशोरों में पुरुषों और महिलाओं के लिए प्रजनन संबंधी परामर्श और/या संरक्षण विकल्प प्रस्तुत किए जाने चाहिए।
कीमोथेरेपी बचपन में होने वाले एएलएल का एक प्रमुख इलाज है। इलाज में दवाइयों का संयोजन शामिल है। इसे पूरा होने में 2 से 3 वर्ष का समय लगता है।
इलाज आमतौर पर एक आउट पेशेंट के आधार पर किया जाता है। लेकिन कई बार ऐसा भी हो सकता है कि रोगी को अस्पताल में रहने की ज़रूरत पड़े।
अमेरिका में कई कैंसर केंद्र और अस्पताल एएलएल का इलाज करते हैं। विशिष्ट दवाएँ, खुराक और डिलीवरी का शेड्यूल कुछ हद तक भिन्न हो सकता है। लेकिन इलाज के सिद्धांत समान हैं।
इलाज योजना रोगी की नैदानिक जांच के परिणामों पर निर्भर करेगी।
सेंट्रल वेनस एक्सेस डिवाइस लगवाने के लिए रोगियों को सर्जिकल प्रक्रिया से गुज़रना होगा। यह डिवाइस सुई की आवश्यकता को कम करता है। डिवाइस के माध्यम से लेबोरेट्री जाँचों के लिए खून लिया जा सकता है और नसों में (आईवी) दवाएँ, द्रव्य, रक्त उत्पाद और पोषण प्रदान किए जा सकते हैं। इलाज पूरा हो जाने के बाद उसे निकाल दिया जाएगा।
इलाज के दौरान रोगियों को स्कूल से अवकाश लेना पड़ सकता है। लेकिन इलाज केंद्र, स्कूल, माता-पिता और छात्र एक साथ काम कर सकते हैं ताकि छात्र जितना संभव हो अध्ययन कर सके।
चिकित्सक व्यक्तिगत रोगियों के जोखिम समूह के आधार पर उनके लिए उपयुक्त इलाज निर्धारित करने में अत्यधिक सक्षम बन रहे हैं।
जोखिम समूह इस संभावना को संदर्भित करता है कि रोगी के कैंसर पर या तो इलाज (जिस पर प्रभाव न पड़े) का प्रभाव नहीं पड़ेगा, या यह इलाज (रोग का वापस आना) की प्रारंभिक प्रतिक्रिया के बाद वापस आ जाएगा। वापस आ चुके या प्रभाव नहीं पड़ने वाले एएलएल के लिए इलाज के विकल्प हैं।
इलाज केंद्र के आधार पर जोखिम समूहों के अलग-अलग नाम होते हैं। सामान्य तौर पर, इन जोखिम समूहों को निम्न, मानक, उच्च और बहुत उच्च कहा जाता है।
कीमोथेरेपी की विधि और दवाई के प्रकार बच्चे के जोखिम समूह पर निर्भर करते हैं। जैसे कि, उच्च-जोखिम वाले खून का कैंसर (ल्यूकेमिया) से पीड़ित बच्चों और को किशोरों को कम जोखिम वाले एएलएल से पीड़ित बच्चों की तुलना में आमतौर पर अधिक कैंसर रोधी दवाएँ और/या अधिक खुराकें प्राप्त होंगी।
कुछ स्थितियों में, इलाज में लक्षित इलाज, प्रतिरक्षा बढ़ाने का उपचार (इम्यूनोथेरेपी) और हेमेटोपोएटिक कोशिका प्रत्यारोपण (जिसे बोन मैरो ट्रांसप्लांट या स्टेम सेल ट्रांसप्लांट के रूप में भी जाना जाता है) भी शामिल हो सकता है।
जोखिम समूहों का निर्धारण निम्नलिखित द्वारा किया जाता है:
चिकित्सक इलाज की सूचना देने के लिए जानकारी एकत्र करते हैं।
रोगी में कीमोथेरेपी, द्रव्य पहुँचाने और उसके खून के नमूने लेने के लिए उसके शरीर में सब्क्यूटेनियस पोर्ट या अन्य वीनस एक्सेस डिवाइस पहुँचाने के लिए उसे सर्जरी से गुजरना होगा।
इस चरण का लक्ष्य बोन मैरो और खून में मौजूद खून का कैंसर (ल्यूकेमिया) कोशिकाओं को नष्ट करने के लिए विभिन्न कीमोथेरेपी के संयोजन का उपयोग करके कैंसर-मुक्त करना या बीमारी को दूर करना है। यह चरण बहुत ही मुश्किल होता है इसलिए रोगी को अस्पताल में रहने की आवश्यकता पड़ सकती है।
रीढ़ की हड्डी के आसपास पानी में मौजूद खून का कैंसर (ल्यूकेमिया) कोशिकाओं को नष्ट करने के लिए केंद्रीय तंत्रिका तंत्र (सीएनएस) सैंक्चुअरी थेरेपी दी जा सकती है।
चिकित्सक यह पता लगाने के लिए कि थेरेपी के साथ आगे कैसे बढ़ना है, यह देखेंगे कि कैंसर के शुरूआती इलाज के साथ खून का कैंसर (ल्यूकेमिया) पर कितना असर पड़ा है।
इस अधिक गहन चरण के लक्ष्य में उन शेष कोशिकाओं को नष्ट करने के लिए दवाओं का विभिन्न संयोजन शामिल है, ताकि खून का कैंसर (ल्यूकेमिया) दुबारा वापस न आए। इसके लिए अस्पताल में रहने की आवश्यकता पड़ सकती है।
फिलाडेल्फिया गुणसूत्र-पॉज़िटिव एएलएल से पीड़ित रोगियों को इस चरण के दौरान इमेटिनिब प्राप्त हो सकती है।
यदि पहले 2 चरणों के बाद खून का कैंसर (ल्यूकेमिया) का पता न रहे, तो रखरखाव थेरेपी शुरू की जा सकती है। इसका लक्ष्य, कीमोथेरेपी दवाओं के संयोजन का उपयोग करके किसी भी शेष बची खून का कैंसर (ल्यूकेमिया) कोशिका को नष्ट करना है, जो पहले इंडक्शन और कंसोलिडेशन चरणों के बाद शेष रह सकती है।
इसमें रोगियों को उच्चस्तरीय कीमोथेरेपी के चक्रों के साथ, जिसे फिर से तेज़ कीमोथेरेपी देना भी कहा जाता है, साप्ताहिक कीमोथेरेपी और खून की जाँच होने की संभावना है।
एएलएल के इलाज के पहले 9 महीने आमतौर पर काफी मुश्किल होते हैं। अक्सर रोगी पहले 9 महीनों के बाद ही स्कूल वापस जा सकते हैं।
रोगी हर 4 महीने में एक बार अनुवर्ती दौरों के लिए वापस आएगा।
इन दौरों में निम्नलिखित शामिल हो सकते हैं:
अनुवर्ती दौरे बदलकर हर 6 महीने में एक बार हो सकते हैं।
अनुवर्ती दौरे बदलकर साल में एक बार हो सकते हैं।
एएलएल के इलाज के 3 चरण हैं और इसे पूरा करने में लगभग 2 से 3 साल का समय लगता है।
कुछ स्थितियों में, चिकित्सक इलाज के अतिरिक्त विकल्पों की अनुशंसा कर सकते हैं।
लक्षित इलाज में उन दवाओं का उपयोग होता है जो कैंसर कोशिकाओं की तलाश करती हैं और आसपास की सामान्य कोशिकाओं को हानि पहुँचाए बिना उन पर हमला करती हैं। इस प्रकार की थेरेपी केवल तभी संभव होती है जब कैंसर में पहचान योग्य जीन (वंशाणु) मौजूद होते हैं और जो उपलब्ध लक्षित दवाओं पर अनुकूल प्रतिक्रिया दिखाते हैं।
लक्षित इलाज की दवाओं में इमैटिनिब या डेसाटिनिब को फिलाडेल्फिया गुणसूत्र-पॉज़िटिव एएलएल और फिलाडेल्फिया-जैसे एएलएल के इलाज में प्रभावी दिखाया गया है।
रुक्सोलिटिनिब का उपयोग एक प्रकार के एएलएल के इलाज के लिए किया जा सकता है जिसे फिलाडेल्फिया-जैसा एएलएल कहा जाता है।
प्रतिरक्षा बढ़ाने का उपचार (इम्यूनोथेरेपी) कैंसर इलाज का वह प्रकार है जिसमें कैंसर से लड़ने के लिए प्रतिरक्षा प्रणाली का उपयोग किया जाता है। सामान्य तौर पर, प्रतिरक्षा बढ़ाने का उपचार (इम्यूनोथेरेपी) कैंसर कोशिकाओं को खोजने में प्रतिरक्षा प्रणाली की मदद करके काम करते हैं। तब यह कैंसर कोशिकाओं पर हमला कर सकता है और/या कैंसर के प्रति प्रतिक्रिया करने के लिए प्रतिरक्षा प्रणाली की क्षमता को बढ़ा सकता है।
प्रतिरक्षा बढ़ाने का उपचार (इम्यूनोथेरेपी) में मोनोक्लोनल एंटीबॉडी दवा जैसे कि ब्लिनेटुमोमैब, इनोटुज़ुमैब ओज़ोगैमिकिन और रिटुक्सीमैब शामिल हो सकती है। किमेरिक एंटीजन रिसेप्टर (CAR) टी सेल, जैसे कि टिसजेनलेक्ल्यूसेल, भी एक संभावित इलाज हो सकता है।
हेमेटोपोएटिक कोशिका प्रत्यारोपण (जिसे बोन मैरो ट्रांसप्लांट या स्टेम सेल ट्रांसप्लांट के रूप में भी जाना जाता है) की सलाह उन बच्चों के लिए दी जा सकती है जिसमें खून के कैंसर (ल्यूकेमिया) के वापस आने की अधिक संभावना है या जिनके एएलएल पर इलाज का असर नहीं हो रहा है। रोगियों को चिकित्सा के दृष्टिकोण से सक्षम होना चाहिए और उनके पास एक उपयुक्त डोनर होना चाहिए।
चिकित्सक यह तय करने के लिए कि रोगी को प्रत्यारोपण की आवश्यकता है या नहीं, कभी-कभी यह देखते हैं कि इंडक्शन कीमोथेरेपी ने रोगी पर कितनी अच्छी तरह काम किया है।
एएलएल इलाज में रेडिएशन का उपयोग शायद ही कभी किया जाता है। यह उन मामलों में दिया जा सकता है जहाँ एएलएल मस्तिष्क, रीढ़ के अंदर की नस, या वीर्यकोष में फैल गया है। 2019 के एक अध्ययन से पता चला है कि एएलएल के लिए केंद्रीय तंत्रिका तंत्र पर रेडिएशन को छोड़ा जा सकता है।
रोगियों को हिमेटोपोएटिक कोशिका प्रत्यारोपण (आमतौर पर बोन मैरो ट्रांसप्लांट या स्टेम सेल ट्रांसप्लांट के रूप में भी जाना जाता है) करवाने को तैयार करने के लिए रेडिएशन भी दिया जा सकता है।
दुष्प्रभावों का पहले से अनुमान लगाना कठिन होता है। वे दवाई पर और किसी व्यक्ति के इस पर प्रतिक्रिया के तरीके पर निर्भर करते हैं। एक ही दवाई के लिए अलग-अलग लोगों की अलग-अलग प्रतिक्रियाएँ हो सकती हैं।
एएलएल इलाज के किसी भी चरण के दौरान दुष्प्रभाव हो सकते हैं। इलाज के पहले सप्ताह (इंडक्शन चरण) सबसे मुश्किल होते हैं और गंभीर दुष्प्रभाव उत्पन्न होने की सबसे अधिक संभावना होती है। इन दुष्प्रभावों के लिए इलाज मौजूद हैं।
दुष्प्रभावों में निम्नलिखित शामिल हो सकते हैं:
एएलएल से पीड़ित लगभग 98% बच्चों में इलाज शुरू हो जाने के बाद कुछ ही सप्ताह में कैंसर-मुक्त होने की प्रक्रिया में सुधार आ जाता है।
एएलएल से पीड़ित 90% से अधिक बच्चों को कैंसर-मुक्त किया जा सकता है। रोगियों को लगभग 5 साल तक सुधार की स्थिति में रहने के बाद कैंसर-मुक्त माना जाता है।
कम जोखिम वाले समूह में एएलएल रोगियों की जीवित रहने की दर 95% से अधिक हो सकती है।
अगर रोगी किसी ऐसे प्रकार के एएलएल से ग्रस्त हैं जो इलाज पर कोई प्रतिक्रिया नहीं दिखाता है (जिस पर प्रभाव न पड़े) या जो इलाज के बाद वापस आ जाता है (पुनरावर्तन), तो चिकित्सीय टीम इलाज विकल्पों पर चर्चा करेगी।
कुछ एएलएल रोगियों में देर से दिखाई देने वाले प्रभाव हो सकते हैं। देरी से दिखाई देने वाला प्रभाव एक स्वास्थ्य-संबंधी समस्या है जो इलाज समाप्त होने के कई महीनों या वर्षों बाद दिखाई देती है।
कैंसर के इलाज के बाद कैंसर रोगियों को उनके उपचार केंद्र देखभाल टीम और/या समुदाय में प्राथमिक देखभाल चिकित्सक के निर्देशों का पालन करना चाहिए। देरी से दिखाई देने वाले प्रभावों का अक्सर इलाज किया जा सकता है या कुछ स्थितियों में उन्हें रोका जा सकता है।
अलग-अलग इलाजों के अलग-अलग देरी से दिखाई देने वाले प्रभाव हो सकते हैं। सभी रोगियों में देरी से दिखाई देने वाले प्रभाव नहीं होंगे। जिन रोगियों ने समान इलाज कराया था, वे अलग-अलग देरी से दिखाई देने वाले प्रभाव अनुभव कर सकते हैं।
एएलएल रोगियों को निम्न जोखिम हो सकता है:
वर्तमान जाँच-विज्ञान उन बच्चों के लिए अधिक प्रभावी इलाज विकसित करने पर केंद्रित है जिनके कैंसर पर मूल चिकित्सा का कोई असर नहीं होता है।
शोधकर्ता उन इलाजों को विकसित करने पर भी ध्यान केंद्रित कर रहे हैं जो थेरेपी के दौरान बहुत अधिक दुष्प्रभाव पैदा नहीं करते हैं और कैंसर से बचे लोगों पर देरी से दिखाई देने वाले प्रभाव बहुत अधिक नहीं दिखाई देते।
—
समीक्षा की गई: फ़रवरी 2020