Група вебсайтів St. Jude
Відкрийте для себе наші передові наукові дослідження, медичну допомогу світового рівня, кар’єрні можливості та багато іншого.
Головна сторінка Дитячої дослідницької лікарні St. Jude
- Кар’єрні можливості
- Освітня та просвітницька діяльність

- Збір коштів
-
Види дитячого раку
Ознайомтеся з вичерпною інформацією про дитячий і підлітковий рак.
-
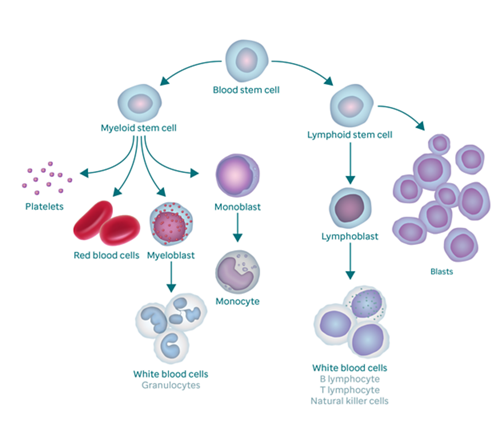
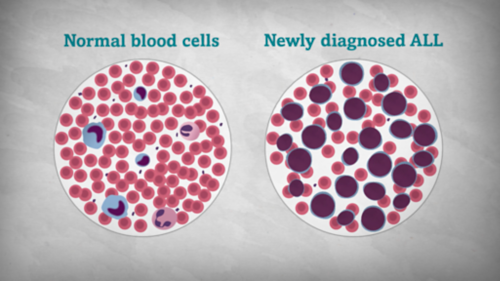
Захворювання крові
Знайдіть інформацію про типи захворювань крові у дітей та підлітків.
-
Інфекційні захворювання
Дізнайтеся більше про інфекційні захворювання у дітей та підлітків.
Методи лікування, аналізи та процедури
Дізнайтеся про методи лікування, аналізи, процедури, ліки та побічні ефекти.
Дізнайтеся про орієнтування в питаннях медичної допомоги та управління медичною допомогою дітям та підліткам.
- Команда педіатричної допомоги
- Орієнтування в питаннях охорони здоров’я
- Клінічна допомога та догляд вдома
- Лікувальне (дієтичне) харчування
- Профілактика та контроль інфекцій
- Управління ліками
- Спадковий ризик та генетичний аналіз
- Психологія та послуги з психічного здоров'я
- Реабілітаційні послуги
- Паліативна допомога (симптоматична терапія та підтримувальний догляд)
- Кінець життя
Емоційна підтримка та повсякденне життя
Дізнайтеся про емоційну підтримку та ресурси, які допоможуть у повсякденному житті.
Дізнайтеся більше з відео, блогів, історій та інших ресурсів.